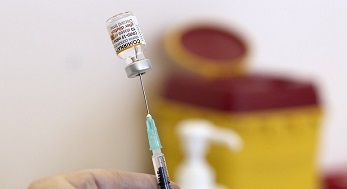
Com a autorização do Ministério da Saúde para que crianças de 5 a 11 anos sejam vacinadas contra a Covid-19, os municípios terão de seguir 17 recomendações definidas pela Anvisa (Agência Nacional de Vigilância Sanitária) para imunizar o público infantil.
Em uma delas, a Anvisa pede que seja evitada a vacinação das crianças em postos de vacinação na modalidade drive-thru. De acordo com a autarquia, a imunização do público infantil deve ser realizada em ambiente específico e segregado da vacinação de adultos, que seja acolhedor e seguro para as crianças.
A Anvisa também estabeleceu que a sala em que se dará a aplicação de vacinas contra o novo coronavírus em crianças seja exclusiva para a aplicação desse imunizante, não sendo aproveitada para a aplicação de outras vacinas, ainda que pediátricas.
Quando houver vacinação em comunidades não urbanas, como aldeias indígenas, a Anvisa sugere que a imunização de crianças seja feita em dias separados, não coincidentes com a de adultos.
Outra diretriz da agência diz que a vacina da Covid-19 para crianças não deve ser administrada ao mesmo tempo que outras vacinas do calendário infantil, por precaução. A Anvisa recomenda um intervalo de 15 dias para a aplicação de outro imunizante.
A instituição recomenda também que as crianças sejam acolhidas e permaneçam no local em que a vacinação ocorrer por pelo menos 20 minutos após a aplicação, facilitando que sejam observadas durante esse breve período.
Reações à vacinação
A agência formulou uma diretriz recomendando que os profissionais de saúde, antes de aplicarem a vacina, informem ao responsável que acompanha a criança os principais sintomas esperados no local da injeção — dor, inchaço e vermelhidão — e outras reações que podem ocorrer — como febre, fadiga, dor de cabeça, calafrios, dor muscular e dor nas articulações.
Segundo a Anvisa, os pais ou responsáveis têm que ser orientados a procurar um médico se a criança apresentar dores repentinas no peito, falta de ar ou palpitações após a aplicação da vacina.
Para evitar a ocorrência de efeitos adversos à vacinação, a autarquia pede que a vacinação das crianças seja iniciada após treinamento completo das equipes de saúde que farão a aplicação do imunizante, já que a grande maioria das reações pós-vacinação é decorrente da administração do produto errado à faixa etária, da dose inadequada e da preparação errônea do produto.
De todo modo, a Anvisa frisa que centros ou postos de saúde e hospitais infantis estejam atentos e treinados para atender e captar eventuais reações adversas em crianças de 5 a 11 anos após tomarem a vacina.
Doses devem chegar na próxima semana
Neste mês, a Pfizer/BioNTech vai enviar ao Brasil 3,7 milhões de doses de vacina para aplicação em crianças. Os imunizantes chegarão em três voos, cada um com 1,248 milhão de doses. O primeiro deles, de acordo com uma previsão apresentada pelo Ministério da Saúde, deve chegar na próxima quinta-feira (13). Os outros dois carregamentos, nos dias 20 e 27.
A vacinação de crianças será administrada em duas doses de 10 microgramas com oito semanas de intervalo entre cada uma. Trata-se de um terço da dose administrada a adolescentes e a adultos. Segundo a Pfizer/BioNTech, o nível de dose foi cuidadosamente selecionado com base em dados de segurança, tolerabilidade e imunogenicidade.
De acordo com a Anvisa, as crianças que completarem 12 anos entre a primeira e a segunda dose devem concluir o esquema vacinal com o imunizante pediátrico da Pfizer/BioNTech.
O frasco da vacina para crianças virá com uma coloração diferenciada, com tampa e rótulo de cor laranja, para que possa ser distinguido da formulação já utilizada hoje em indivíduos com 12 anos ou mais.
Segundo a Anvisa, os profissionais de saúde, antes de aplicarem a vacina, terão de mostrar o frasco com a dose específica para o público infantil ao responsável que acompanha a criança, assim como a seringa a ser utilizada, de 1 mL.
Para evitar equívocos, a Anvisa sugere a implementação de um plano de comunicação sobre essas diferenças de cor entre os produtos, incluindo a utilização de redes sociais e estratégias mais visuais que textuais.
CoronaVac em avaliação
No momento, apenas a vacina da Pfizer/BioNTech está aprovada para aplicação no público infantil, mas a Anvisa analisa um pedido feito pelo Instituto Butantan para o uso da CoronaVac em crianças e adolescentes de 3 a 17 anos. O Butantan diz que já tem reservados 12 milhões de doses para aplicação em crianças e adolescentes.
Na sexta-feira (7), o instituto divulgou um dossiê com artigos sobre a eficácia da CoronaVac, incluindo um publicado no periódico científico The Lancet Infectious Diseases que constatou que a vacina é segura para a população de 3 a 17 anos e pode induzir uma forte produção de anticorpos no grupo pediátrico.
O estudo foi feito na China e avaliou 550 crianças e adolescentes (71 na fase 1 e 479 na fase 2) para medir a segurança, a tolerabilidade e a imunogenicidade da aplicação de duas doses da CoronaVac com um intervalo de 28 dias entre elas.
Um grupo tomou a vacina enquanto o outro recebeu placebo com hidróxido de alumínio, adjuvante não nocivo ao organismo presente na fórmula do imunizante. As análises mostraram que a vacina foi capaz de gerar anticorpos em 96% dos voluntários 28 dias após a segunda dose.
As reações adversas foram de leves a moderadas, sendo dor no local da aplicação e febre as mais comuns, com desaparecimento dos sintomas em até 48 horas. Segundo o estudo, 27% dos participantes relataram efeitos colaterais. Houve apenas um caso de evento adverso grave, não associado à vacina — uma criança teve pneumonia após receber placebo.
Fonte: www.noticias.r7.com / Postado em 10/01/2022 – 02H00 (ATUALIZADO EM 10/01/2022 – 09H09)